Forças intermoleculáres
Ligações
Tipos
- Ligações polares: podem ser hidrogênio ou polar
- Ligações não polares
Forças
Entre moléculas: força elétrica (carga)
Entre neutron e proton: força forte e fraca
Interações
Elétricas

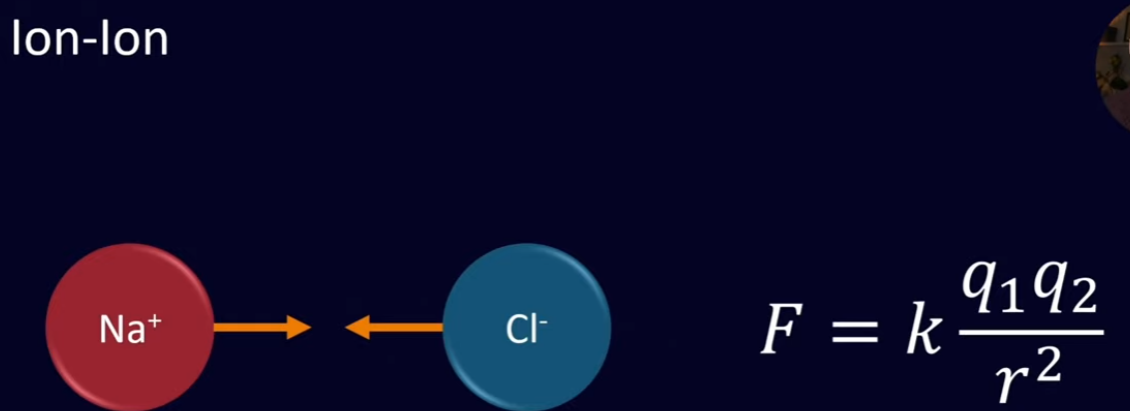
Ion-Ion
Quando um possui carga positiva e outro negativa
Dipolo
Diz-se quando compartilha-se elétron de forma desigual
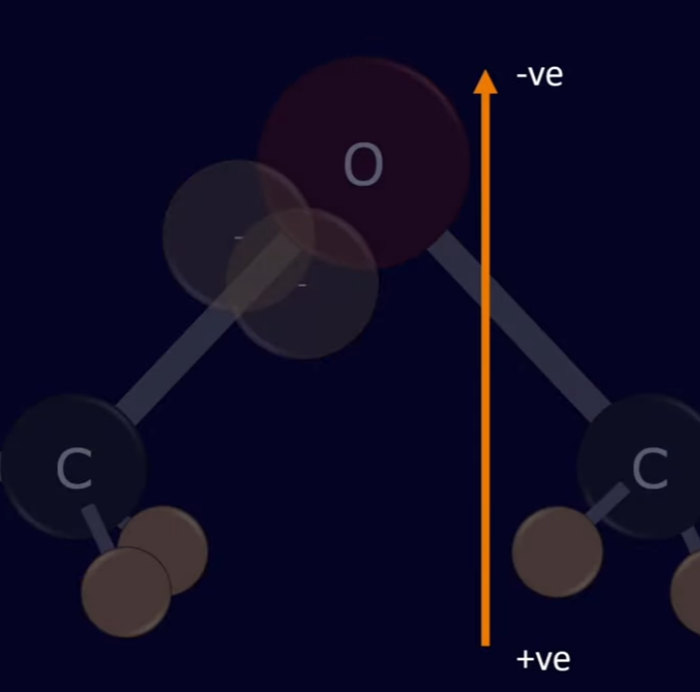
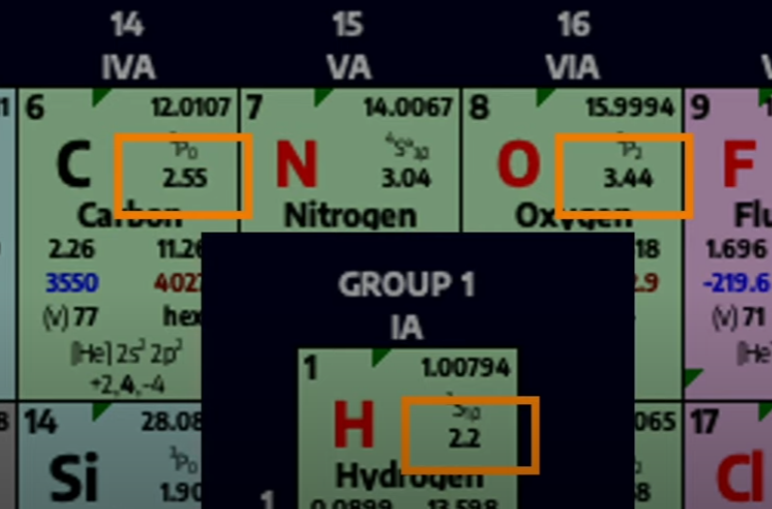 Por exemplo olhando na tabela periódica o valor eletronegatividade caso a diferença for maior que 0.5 normalmente se chama de ligação dipolo e o compartilhamento dos elétrons fica mais perto do átomo com maior eletronegatividade, por exemplo entre carbono e oxigênio:
Por exemplo olhando na tabela periódica o valor eletronegatividade caso a diferença for maior que 0.5 normalmente se chama de ligação dipolo e o compartilhamento dos elétrons fica mais perto do átomo com maior eletronegatividade, por exemplo entre carbono e oxigênio:
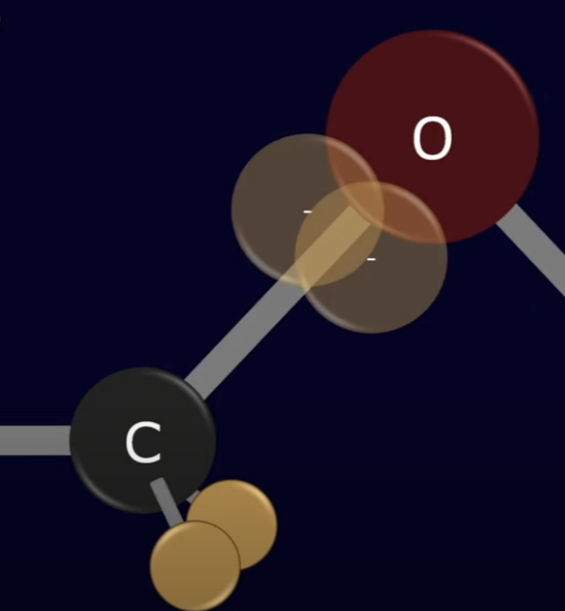
E se observar, existem mais elétrons na parte de cima do que de baixo, como se fosse um polo mais negativo carregado e abaixo um polo positivo
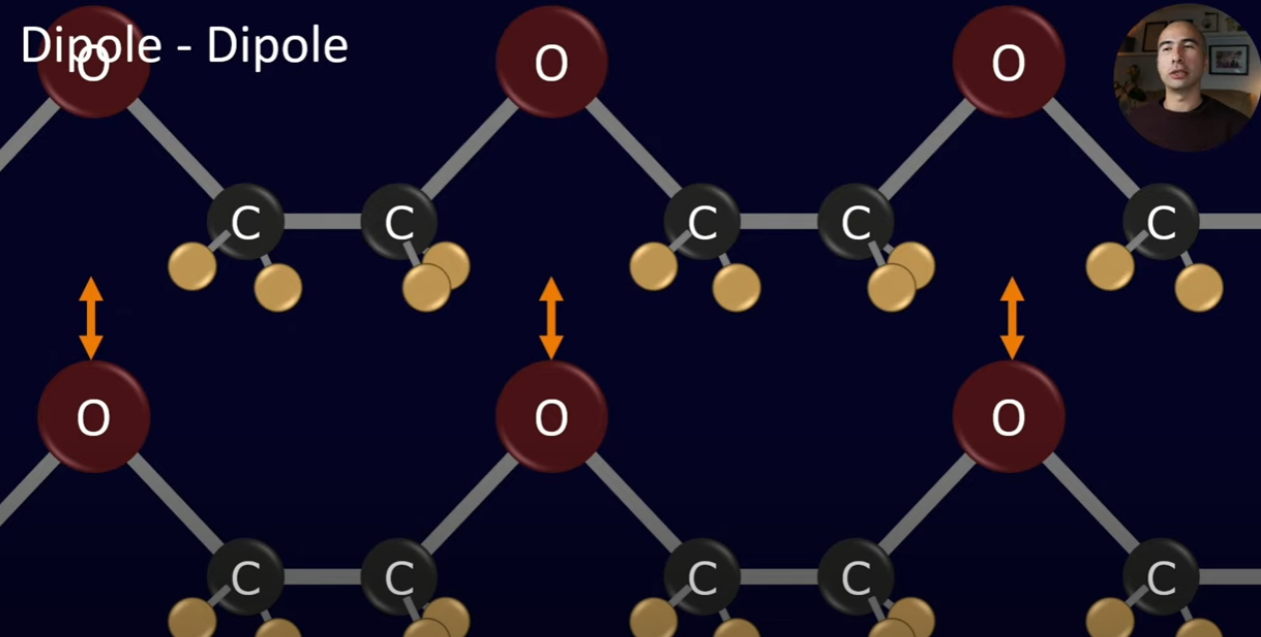
Dipolo-dipolo
Se unirmos o dipolo com outro dipolo
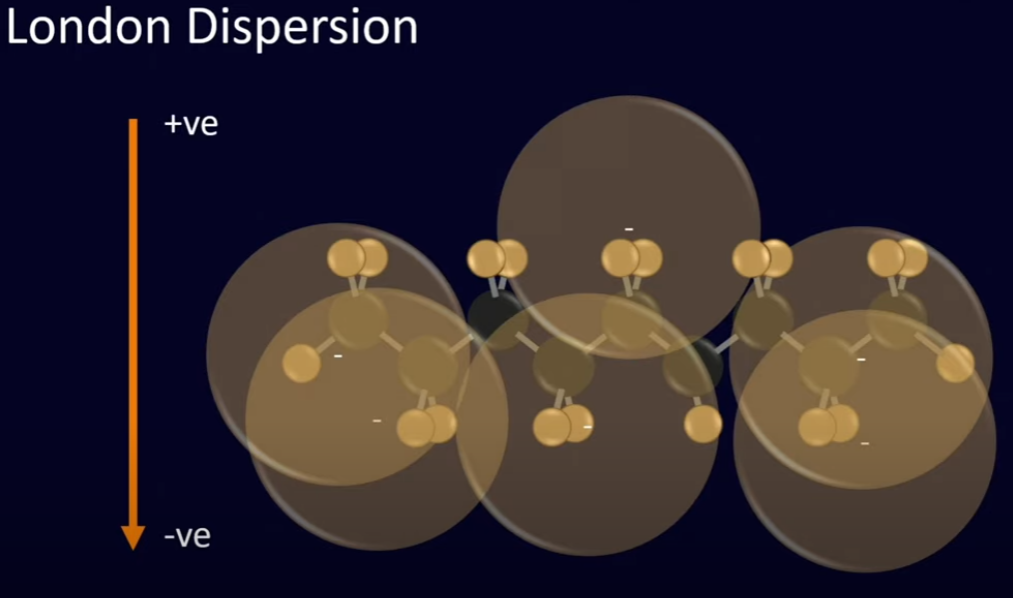
Dispersão de London
Os elétrons possuem movimentos flutuantes e erráticos e uma chance aleatória pode ocorrer um dipolo por um breve momentâneo mas que basta para iniciar atratividade nas moléculas próximas
É a força mais fraca